Генетические заболеванияЦелиакия (часть первая) Целиакия (другое название глютеновая энтеропатия) - это наследственное аутоиммунное заболевание тонкой кишки, которое встречается у людей разного возраста, даже у детей. Симптомы включают: хронический понос, задержку физического развития (у детей), усталость, однако могут присутствовать и другие признаки, влияющие на деятельность других органов и систем. Все большая доля случаев целиакии диагностируется еще до появления симптомов, в результате применения массового скрининга. Как считается, заболевание встречается у 1 человека с 1750-1105 в США. Целиакия возникает в связи с негативной реакцией организма на глиадин - это проламин (белок клейковины (глютена)), содержащийся в пшенице. Подобные белки обнаружены также в растениях, которые относятся к трибу пшеничных (Triticeae tribe), который включает в себя другие зерновые культуры, такие как ячмень и рожь.
 Под влиянием глиадина, а именно трех пептидов которые были обнаружены в проламине, фермент тканевой трансглутаминазы меняет белок, а иммунная система вступает в перекрестную реакцию с тканями тонкой кишки, вызывая воспалительные реакции, следствием которых является повреждение ворсинок тонкой кишки (так называемая атрофия ворсинок). Это препятствует усвоению питательных веществ организмом, ведь кишечные ворсинки ответственны за поглощение необходимых веществ. Единственным известным способом лечения есть соблюдение постоянной безглютеновой диеты. Стоит отметить, что хотя болезнь вызвана реакцией на протеины, содержащиеся в пшенице, однако это заболевание нельзя назвать аналогичным аллергии на пшеницу. Под влиянием глиадина, а именно трех пептидов которые были обнаружены в проламине, фермент тканевой трансглутаминазы меняет белок, а иммунная система вступает в перекрестную реакцию с тканями тонкой кишки, вызывая воспалительные реакции, следствием которых является повреждение ворсинок тонкой кишки (так называемая атрофия ворсинок). Это препятствует усвоению питательных веществ организмом, ведь кишечные ворсинки ответственны за поглощение необходимых веществ. Единственным известным способом лечения есть соблюдение постоянной безглютеновой диеты. Стоит отметить, что хотя болезнь вызвана реакцией на протеины, содержащиеся в пшенице, однако это заболевание нельзя назвать аналогичным аллергии на пшеницу. Для обозначения этого расстройства используется несколько других названий, в том числе целиатичная болезнь (cœliac с лигатурой œ), целиатическое спру (c (o) eliac, нарушение всасывания пищи), однако это нетропическое спру, а эндемическое, вызванное глютеновой (клейковина) энтеропатией и непереносимостью клейковины. Термин целиакия происходит от греческого κοιλιακός (koiliakόs, "брюшной"), он был введен в обращение в 19 веке, учитывая переводы робот древнегреческого врача Аретея с Каппадокии (Aretaeus of Cappadocia). Признаки и симптомы Тяжелая форма целиакии приводит к появлению характерных симптомов: бледности, поноса, жирного стула (стеаторея) и потери веса или неспособности набрать вес (у маленьких детей). Люди со средней формой целиакии могут иметь признаки, более скрытые и встречаться в других органах, а не в самом кишечнике. Кроме того, возможен вариант бессимптомного течения болезни. У многих взрослых с «изящной» болезнью наблюдается только усталость или анемия. Желудочно-кишечные признаки Диарея, которая характеризует целиакию является бледноватой, продолжительной и сопровождается неприятным запахом. Кроме того, характерными при болезни являются: - боль в животе и спазмы; - вздутие живота с повышением внутрибрюшного давления и объема (который, как считается, возникает в связи с ферментативным образованием кишечных газов); - язвы ротовой полости; - поскольку прогрессирует поражения ворсинок тонкой кишки, то может развиваться непереносимость лактозы (гиполактазия). Часто сначала эти симптомы связывают с синдромом раздраженного кишечника (СРК) и только позднее определяют наличие целиакии. У незначительного числа пациентов с симптомами СРК их причиной является целиакия, однако скрининг для определения целиакии рекомендуется проходить всем людям с симптомами СРК. Целиакия приводит к повышению риска появления, как аденокарциномы (рака тонкой кишки), так и лимфомы тонкой кишки (ассоциированная с энтеропатией Т-клеточная лимфома или АЕТЛ (англ. EATL)). Этот риск уменьшается при условии применения соответствующей диеты. У больных на поздних стадиях, без должного лечения появляются другие осложнения, такие как язвенное воспаление тонкой кишки (образование язв в тонкой кишке) и ее сужение вследствие рубцевания через непроходимость тонкой кишки. Симптомы связаны с мальабсорбцией Изменения в стенке тонкой кишки (атрофия ворсинок) уменьшают ее способность всасывать питательные вещества, минералы и жирорастворимые витамины A, D, Е и К. * Неспособность поглощать углеводы и жиры может привести к потере веса (или задержки роста у детей), усталости или нехватки энергии. * Анемия может развиваться в нескольких направлениях: нарушение всасывания железа при мальабсорбции может привести к железодефицитной анемии, а нарушение всасывания фолиевой кислоты и витамина В12 ко мегалобластной гиперхромной (витаминодефицитной) анемии. * Мальабсорбция кальция и витамина D (и соответственно вторичного гиперпаратиреоза) может вызвать остеопению (снижение минеральной плотности костей) или остеопороз (хрупкость костей и повышенный риск их переломов вследствие уменьшения их массы). * Небольшая доля пациентов имеет аномальную коагуляцию в связи с дефицитом витамина К и повышенный риск возникновения внезапных кровотечений. * Целиакия также связана с синдромом повышенного размножения бактерий в тонкой кишке (Small bowel bacterial overgrowth syndrome), который может ухудшить тяжесть мальабсорбции или быть причиной ее возникновения, несмотря на лечение. Разное
Целиакию связывают с рядом различных симптомов. Во многих случаях очень трудно понять, заболевания вызвано действием клейковины или это расстройство связано с другими причинами. Дефицит иммуноглобулина А (ІgA) характерен для 2,3% пациентов с целиакией, однако вместе с тем, это нарушение увеличивает вероятность возникновения целиакии в 10 раз. Относительно других особенностей то при этом дефиците существенно повышается риск появления инфекций и аутоиммунных заболеваний. Герпетиформный дерматит - это расстройство, которое влечет зуд кожи связан с нарушением действие 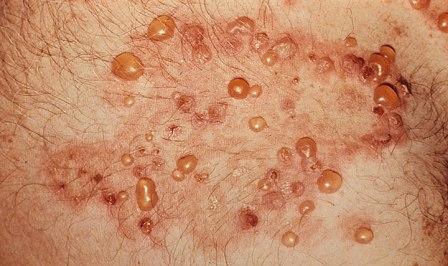 фермента трансглутаминазы в коже. Изменения строения тонкой кишки при этом идентичны тем, которые возникают при целиакии, и могут быть вызваны реакцией организма на клейковину, даже если нет никаких желудочно-кишечных симптомов. фермента трансглутаминазы в коже. Изменения строения тонкой кишки при этом идентичны тем, которые возникают при целиакии, и могут быть вызваны реакцией организма на клейковину, даже если нет никаких желудочно-кишечных симптомов. Задержка физического развития и (или) полового созревания в подростковом возрасте может происходить даже без явных симптомов нарушения деятельности кишечника или тяжелых нарушений процессов питания. Для того, чтобы оценить отклонения в физическом развитии часто рекомендуют провести скрининговое обследование органов брюшной полости. Периодические выкидыши и бесплодие (причина которого не обнаружена). Гипоспленизм (Hyposplenism) (размер селезенки меньше нормального значения) - характерно примерно для трети случаев заболевания целиакией и может приводить к нарушению функций селезенки, которые направлены на защиту организма от воздействия бактерий. Нарушение печеночных проб (биохимического анализа крови), которые могут быть случайно обнаружены при биохимическом анализе крови; Целиакия связана с рядом других заболеваний, многие из которых являются аутоиммунными нарушениями. Сахарный диабет 1 типа, аутоиммунный тиреоидит, первичный билиарный цирроз печени и микроскопический колит. Иногда обнаруживают связь целиакии с заболеваниями другой группы (однако эта связь на сегодня остается спорным вопросом), для которой характерной чертой является наличие антител анти-глиадину (выявленных с помощью проведения старых неспецифических тестов), однако эти заболевания не связаны с тонким кишечником. Иногда, эти заболевания тоже лечатся уменьшением уровня употребления клейковины. К ним относиться мозжечковая атаксия, периферическая нейропатия, шизофрения и аутизм. Другие зерновые Некоторые сорта пшеницы и крупы из них (например, такие как полба, манная крупа и твердые сорта пшеницы), а также другие связанные с ними виды, такие как ячмень, рожь, тритикале (новая озимая или яровая злаковая растение, искусственно созданная селекционерами скрещиванием ржи с пшеницей) и камут, также могут вызывать симптомы целиакии. Небольшая доля больных целиакией реагируют также на овес. Наиболее вероятно, что овес вызывает симптомы целиакии в связи с перекрестным опылением другими зерновыми на полях или в каналах распределения. То есть, овес не рекомендуется употреблять людям с этим заболеванием. Другие зерновые, такие как кукуруза, просо, сорго, ТЭФ, обычный и дикий рис - безопасны для пациентов, так же как незлаковые культуры, такие как амарант, лебеда или гречка. Незерновые, богатые углеводами продукты, такие как картофель и бананы не содержат глютена и не вызывают симптомы заболевания. Патофизиология Считается, что целиакия является полифакториальной болезнью, поскольку ее возникновения может вызвать более чем один генетический фактор, а для проявления ее у пациента необходимо наличие также более чем одного фактора. Почти все пациенты имеют HLA-DQ2 вариант аллели. Однако около 20-30% людей, которые не имеют целиакию, унаследовали HLA-DQ2 аллель. Именно это предполагает необходимость дополнительных факторов для развития болезни. Кроме того, около 5% людей у которых развивается болезнь не имеют гена DQ2. HLA-DQ2 аллель характеризуется неполной пенетрантностью, ведь связанные с болезнью алели гена, появляются у большинства пациентов, однако они присутствуют не во всех случаях, а сами по себе не является достаточной причиной возникновения заболевания. Генетика Подавляющее большинство пациентов с целиакией имеют один из двух типов HLA-DQ. Этот ген является частью II класса антигенов-рецепторов главного комплекса гистосовместимости (MHC class II antigen-presenting receptor), другое название которого человеческий лейкоцитарный антиген. Гены этой системы, отвечают за различение собственных и чужих клеток организмом, т.е. связанные с иммунной системой. Ген, нарушение деятельности которого вызывает целиакию, расположенный на коротком плече шестой хромосомы и называется CELIAC1. На сегодня известно семь вариантов HLA-DQ (DQ2 и DQ4-DQ9). Более 95% больных целиакией имеют наследственную изоформу DQ2 или DQ8. Причина, почему эти гены, вызывают повышение риска возникновения целиакии, заключаются в том, что рецепторы этих генов образуют с пептидами глиадина более сильнаю связь, чем другие антиген-представляющие рецепторы (antigen-presenting receptor). То есть, вероятно, что именно эти формы рецептора, активируют Т-лимфоциты и, соответственно, аутоиммунный процесс. Большинство больных целиакией являются носителями двух генов гаплотипа HLA-DQ2, относящихся к гаплотипу DQ2.5. Этот гаплотип состоит из двух смежных аллелей гена DQA1 * 0501 и DQB1 * 0201, кодирующих две субъединицы, DQ α5 и DQ β2. У большинства людей, эта DQ2.5 изоформа кодируется одной из двух копий 6 хромосомы, унаследованных от родителей. Большинство больных целиакией наследуют только одну копию этого гаплотипа DQ2.5, а некоторые наследуют его от обоих родителей. У последних, риск возникновения целиакии особенно высок, кроме того, они более склонны к появлению различных осложнений. Некоторые люди наследуют DQ2.5 от одного из родителей и часть гаплотипа (DQB1 * 02 или DQA1 * 05) от другого, таким образом, у таких особей риск развития заболевания тоже увеличивается. Реже, люди наследуют DQA1 * 05 аллель от одного из родителей и DQB1 * 02 от другого, это явление называется транс-гаплотипной ассоциацией, и риск возникновения заболевания у этих людей аналогичный тем особям, которые наследуют копию 6 хромосомы с DQ2.5 гаплотипом, но в этом случае, болезнь не считается семейной. Среди больных жителей Европы 6% не имеют DQ2.5 (цис-или транс) или DQ8 (кодирует гаплотип DQA1 * 03: DQB1 * 0302), 4% имеют изоформу DQ2.2, а у 2%,котрые остались отсутствуют DQ2 или DQ8. Распространенность этих генов зависит от географического положения. DQ2.5 очень распространен среди народов Северной и Западной Европы (чаще всего среди басков и ирландцев), части населения Африки и Индии. Однако эти гены вообще не встречаются в странах, находящихся в западной части Тихого океана. DQ8 - более распространен, чем DQ2.5, и чаще встречается среди жителей Южной и Центральной Америки, около 90% людей среди населения американских индейцев являются носителями DQ8, то есть, можно говорить о наличии у них целиакического фенотипа (celiac phenotype). О наличии других генетических факторов, вызывающих целиакию довольно часто сообщают и сегодня, однако частота их появления тоже зависит от географического расположения. Только локусы HLA-DQ встречаются у большинства населения мира. Многие из локусов, как оказалось связаны с другими аутоиммунными заболеваниями. Один ген - LPP (lipoma-preferred partner gene) участвует в адгезии внеклеточного матрикса на поверхности клеток, а несколько измененная его вариация (SNP = rs1464510) увеличивает риск развития заболевания примерно на 30%. Этот ген, часто вызывает целиакию (достоверность р <10-39) у населения Европы и США. .jpg) Проламины Большинство имеющихся в пище белков, отвечающих за иммунную реакцию при целиакии - это проламины. Эти накопительные белки богатые пролином (прол-) и глютамином (-амины), они растворяются в спиртах и устойчивы к протеазам и пептидазам кишечника. Проламины находятся в зерновых культурах, однако различные зерна имеют различные, но связанные проламины: пшеница (глиадин), ячмень (гордеин), рожь (секалин), кукуруза (Зейн), а также незначительное количество белка авенина, который содержится в овсе. Одна область α-глиадина стимулирует клетки мембран энтероцитов кишечника, для того, чтобы пропустить большие молекулы между клетками. Нарушение плотных контактов двух клеток, мембраны которых объединены вместе для формирования практически непроникающего для жидкости барьера, позволяет пептидам, которые больше трех аминокислот попасть в организм. Мембранная утечка пропускает пептиды глиадина, которые стимулируют два уровня иммунных реакций, врожденные и адаптивные (опосредованные клетки Т-хелперы). Один пептид, который резистентный к действию протеазы α-глиадина содержит регион, который стимулирует лимфоциты и приводит к высвобождению интерлейкина 15 (ИЛ-15). Этот врожденный ответ на глиадин имеет результатом реакцию иммунной системы, при которой активируются воспалительные клетки и увеличивается выпуск воспалительных химических веществ. Сильная и наиболее распространенная реакция на глиадин направлена на фрагмент α2-глиадина, состоящего из 33-х аминокислот. Эта реакция происходит у большинства больных целиакией, имеющих DQ2 изоформу. Этот пептид, изменен кишечной трансглутаминазой, имеет высокую плотность перекрытия эпитопов Т-клеток. Это увеличивает вероятность того, что при распознавании Т-клетками DQ2 изоформа будет связываться и дальше будет связанной с пептидом. Глиадин в пшенице является наиболее изученным и наиболее понятным членом этой семьи, однако существуют и другие проламины, которые могут способствовать появлению целиакии, а именно гордеин (из ячменя) и секалин (из ржи). Однако, не все проламины вызывают эту иммунную реакцию и до сих пор продолжаются споры о способности авенина (проламин, который находится в овсе) вызывать реакцию при целиакии. Тканевая трансглутаминаза В большинстве случаев заболевание целиакией в организме больных находят анти-антитела к тканевой трансглутаминазы (ТТГ). Тканевая трансглутаминаза меняет пептиды клейковины на форму, которая вызывает более эффективную иммунную реакцию. Эти пептиды могут изменяться под действием ТТГ двумя способами: дезамидированием или переамидированием. Дезамидирование - это реакция, в процессе которой, при расщеплении ипсилон аминогруппы боковой цепи глютамина образуется остаток глутамата. Переамидирование, встречается втрое чаще дезамидирования. При переамидирование происходит объединение (образование кросс-связей) остатков глутамина (с пептида глиадина) с остатками лизина тканевой трансглутаминазы в процессе реакции, которая катализируеться трансглутаминазой. Объединение может происходить либо внутри или вне активного центра фермента. В последнем случае, образуется устойчивый ковалентно связанный комплекс глиадина и ТТГ. Это приводит к образованию новых эпитопов которые, как полагают, вызывают первичный иммунный ответ, в результате которого образуются аутоантитела против ТТГ. Результаты биопсии пациентов, у которых подозревали целиакию, показывают, что наличие аутоантител (даже если человек еще не имел симптомов заболевания) в большинстве случаев имело следствием развитие болезни в будущем. Аутоантитела находят также у пациентов, страдающих от других аутоиммунных заболеваний, анемии или мальабсорбции, гораздо чаще чем у здорового населения. Ендомизиальные компоненты антител (EMA) к ТТГ, как полагают, направленные на поверхность трансглутаминазы. Наличие этих антител и сегодня используется для подтверждения или опровержения диагноза целиакии. Однако, в 2006 году было проведено исследование, которое показало, что ЭМА-негативные пациенты, больные целиакией, как правило, являются мужчинами старшего возраста, которые имеют более тяжелые брюшные проявления и ниже риск возникновения «нетипичных» симптомов, включая аутоиммунные заболевания. При этом исследовании количество анти-ТТГ антител не коррелирует с тяжестью проявлений в результате повреждения ворсинок. Эти данные в сочетании с проведенным недавно исследованиям показывают, что глиадин имеет собственный компонент, который провоцирует болезнетворную реакцию. Исследователи предполагают, что именно глиадин может быть в большей степени ответственным за первичные проявления целиакии, тогда как ТТГ играет более важную роль при появлении вторичных эффектов, таких как аллергические реакции и вторичные аутоиммунные заболевания. У большинства больных целиакией, анти-ТТГ антитела также распознают ротавирусный белок VP7. Эти антитела стимулируют пролиферацию моноцитов, именно поэтому ротавирусная инфекция может объяснить первоначальную причину процесса пролиферации иммунных клеток. Действительно, на начальном этапе, ротавирусное повреждение кишечника приводит к атрофии ворсинок. Это говорит о том, что вирусные белки могут провоцировать активацию кросреакции организма, при которой производятся анти-VP7. Атрофия ворсинок и мальабсорбция Воспалительный процесс, вызванный Т-клетками, приводит к нарушению структуры и функций слизистой оболочки тонкой кишки и приводит к мальабсорбции, что снижает способность организма усваивать питательные вещества, минералы и жирорастворимые витамины А, D, E и K, которые поступают с пищей. Возможна непереносимость лактозы в связи с снижением поверхности кишечника и сокращением производства лактазы, но обычно эту проблему можно решить при лечении болезни. Были предложены альтернативные причины этого повреждения тканей, они включают в себя: освобождение интерлейкина 15 и активацию иммунной системы пептидом короткой клейковины (p31-43/49). Это вызывает «уничтожение» энтероцитов лимфоцитами в эпителии. Атрофия ворсинок, которую можно увидеть при биопсии может возникать от несвязанных с болезнью причин, таких как тропическая спру (тропическая диарея), лямблиоз и радиационный энтерит. Хотя положительная серология и типичная биопсия являются определенными указателями наличия целиакии, отсутствие реакции на диету может быть основанием для признания этого альтернативного диагноза. Модификаторы риска
Есть много разных теорий относительно того, что определяет, будет ли у генетически впечатлительного человека развиваться целиакия. Основные теории возникновения болезни включают инфекции ротавируса или аденовируса кишечника человека. Некоторые исследования показывают, что курение защищает от появления целиакии во взрослом возрасте. Перспективное и обсервационное исследование 2005 года показало, что затраты времени действия на клетчатку в детстве являются важным модификатором риска. Люди, потреблявшие пшеницу, ячмень или рожь в период до полноценного формирования защитного барьера кишки (в течение первых трех месяцев после рождения) имеют в пять раз выше риск развития целиакии чем те, кто потребляет их после четырех-шести месяцев после рождения. Кроме того, было обнаружено, что риск заболеваемости у тех, кто принимал после шести месяцев с рождения, был только слегка повышен по сравнению с предыдущей группой. Исследование, проведенное в 2006 году, показало, что раннее введение злаков в рацион защищает от появления аллергии на них. Грудное вскармливание также может уменьшить риск возникновения болезни. Анализ показал, что продолжение грудного вскармливания до введения в диету зерновых, содержащих клейковину было связано с 52% снижением риска развития целиакии у детей грудного возраста, однако остается неизвестным или это соотношение сохраняется во взрослом возрасте. Диагностика На сегодняшний день известно несколько тестов, позволяющих точно диагностировать наличие целиакии. Порядок использования тестов устанавливается на основе уровня проявления симптомов. Однако, все испытания теряют свою полезность, если пациент уже придерживается безглютеновой диеты. Деятельность кишечника начинает улучшаться, через несколько недель, после удаления клейковины из рациона, а снижение уровня антител происходит в течение нескольких месяцев. Для особей, которые уже начали соблюдать безглютеновою диету, необходимым может быть повторный вызов симптомов (реакции организма) с помощью употребления продуктов, содержащих клейковину. Это должен быть один прием пищи в день на протяжении 2-6 недель. Только после этого можно осуществлять повторные исследования. 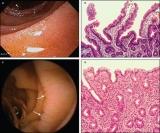 Формируя диагностическую систему, путем комбинации тех результатов, которые можно получить при использовании эндоскопической биопсии (на рис. размещенном слева два верхних изображения - результаты исследований характерные для здорового человека, а два нижних, для человека больного целиакией), исследователи сообщили о 100% чувствительность (при идентификации всех случаев) среди пациентов с высоким индексом подозрения целиакией, с сопутствующей специфичностью 61% (доля ложноположительных результатов 39%). Формируя диагностическую систему, путем комбинации тех результатов, которые можно получить при использовании эндоскопической биопсии (на рис. размещенном слева два верхних изображения - результаты исследований характерные для здорового человека, а два нижних, для человека больного целиакией), исследователи сообщили о 100% чувствительность (при идентификации всех случаев) среди пациентов с высоким индексом подозрения целиакией, с сопутствующей специфичностью 61% (доля ложноположительных результатов 39%).Врачи рекомендуют во время диагностики, пациентам с симптомами, которые указывают на высокий риск присутствия заболевания, или же те, которые имеют положительный анализ крови, пройти эндоскопическую биопсию второй части двенадцатиперстной кишки. Исследование определяет следующие симптомы (которые указывают на высокий риск развития заболевания) как: потеря веса, анемия (гемоглобин менее 120 г / л у женщин или менее 130 г / л у мужчин) или диарея (более трех разового жидкого стула в день). Анализы крови Серологические анализы крови является первоочередным методом исследования необходимым для диагностики целиакии. Антиендомизиальные антитела IgA могут указать на наличие целиакии с чувствительностью и специфичностью 90% и 99% соответственно. Систематический обзор указывает на то, что распространенность целиакии при первичной помощи пациентам с желудочно-кишечными симптомами составляет около 3%. Сначала говорилось, что серология антител трансглутаминазы (anti-tTG) имеет высокую чувствительность (99%) и специфичность (90%) выявление целиакии, однако при систематическом обзоре было установлено, что эти два теста были схожими. Современные анти-tTG анализы полагаются на человеческий рекомбинантный белок в качестве антигена. Первоначально необходимо сделать проверку tTG, как простейший вид исследования. Результаты, вызывающие сомнение должны сопровождаться анализом антител к ендомизиуму. При положительном анализе крови профессионалы рекомендуют пациентам сделать эндоскопию/ гастроскопию и биопсию. Отрицательный результат серологии может также сопровождаться рекомендациями для прохождения эндоскопии и биопсии двенадцатиперстной кишки, если клинические подозрения остаются высокими 1 из 100 "ложно-отрицательных" результатов. Таким образом, биопсия ткани по-прежнему считается «золотым стандартом» при диагностике целиакии. Исторически анализируется наличие трех других антител: анти-ретикулина (АRА), анти-глиадина (АGА) и анти-ендомизиума (EMA). Анализ крови может быть ненадежным источником при диагностике маленьких детей. Исследование анти-глиадина (выполняется более должным образом) используется чаще у детей до пятилетнего возраста. Серологические тесты основаны на реакции иммунной флюоресценции-РИФ (ретикулин, глиадин и ендомизиум) или иммуноферментном анализе-ИФА (глиадин или тканевая трансглутаминаза, tTG). Специалисты рекомендуют параллельно проверять общий уровень IgA в сыворотке крови, поскольку пациенты с дефицитом IgA могут быть не в состоянии вырабатывать антитела, на основе которых базируются эти испытания ("ложно-отрицательные"). У тех пациентов, антитела IgG против трансглутаминазы (IgG-TTG) могут быть диагностическими. Анализ на наличие антител и человеческого лейкоцитарного антигена (лла, англ.HLA) имеют аналогичную точность. Тем не менее, в настоящее время не рекомендуется широко применять анализ HLA для исключения целиакии. Эндоскопия
Для диагностики проводится верхняя эндоскопия с биопсией двенадцатиперстной кишки (выше луковицы двенадцатиперстной кишки) или тонкой кишки. Для врача очень важно получить несколько образцов из двенадцатиперстной кишки (от 4 до 8). Не все участки могут быть повреждены, поэтому если во время биопсии будет взят образец здоровой ткани, то результат будет ложным. У большинства пациентов, которые поражены целиакией при эндоскопии тонкая кишка кажется нормальной, однако наличия одновременно пяти эндоскопических отклонений могут указать на наличие целиакии: ступенчастая ((scalloping) тонкая кишка, малое количество складок, мозаичная слизистая оболочка (вид которой напоминает засушенную, потрескавшуюся грязь), нарушение подслизистой основы, которая покрывает кровяные сосуды и неравенство слизистой. К 1970-м годам, биопсия проводилась путем использованием металлических капсул, которые были оборудованы специальным всасывающим устройством. Эта капсула глоталась и проходила в тонкий кишечник. После рентгеновской проверки ее расположения, активировался всасывающий механизм, который позволял получить образец ткани кишечной стенки, который помещался в капсулу. На практике часто использовали такие капсульные системы, как капсула Ватсона и Кросби-Куглера. Однако сегодня этот метод уже почти полностью заменен волоконно-оптической эндоскопией, чувствительность и точность которой значительно выше. Патология Обычно патологические изменения, характерные для целиакии тонкой кишки классифицируются согласно "Классификации Марша": - 0 стадия - нормальная слизистая оболочка; - 1 стадия - увеличение числа внутренних эпителиальных лимфоцитов. Их количество, как правило, .jpg) превышает 20 лимфоцитов на 100 энтероцитов; превышает 20 лимфоцитов на 100 энтероцитов;- 2 стадия - пролиферация Либеркуновых крипт (crypts of Lieberkuhn) - трубчатых углублений эпителия слизистой оболочки кишечника;
- 3 стадия - частичная или полная атрофия ворсинок; - 4-й стадия - гипоплазия малой архитектуры кишечника. М. Марш предложил такую классификацию в 1992 году, впоследствии, в 1999 году, количество стадий было увеличено до шести. Это было осуществлено через разделение третьей стадии на три подстадии. Однако дальнейшие исследования показали, что эта система не всегда надежна и что изменения, наблюдаемые при целиакии могут быть описаны в одном из трех этапов-A. Состояние здоровья больных целиакией, как уже было сказано, существенно улучшается после вывода из рациона клейковины. Однако большинство специалистов не советует проводить повторную биопсию до тех пор пока не будет улучшения состояния здоровья после изменения рациона. Более подробную информацию об этом заболевании вы можете найти в статье &a <<<
Алькаптонурия
Гистидинемия
Гомоцистинурия
Поликистозная болезнь почек
Cиндром Марфана (Болезнь Марфана)
Анемия Фанкони
Аргининосукцинатная ацидурия
Бета-талассемия
Боковой амиотрофический склероз (часть вторая)
Боковой амиотрофический склероз (часть первая)
Болезнь I клеток
Болезнь Вильсона - Коновалова
Болезнь Гирке
Болезнь Дауна
Болезнь Канавана
Болезнь кленового сиропа
Болезнь Краббе
Болезнь Ниманна - Пика
Болезнь Тея-Сакса (вторая часть)
Болезнь Тея-Сакса (первая часть)
Болезнь Фабри
Болезнь фон Виллебранда
Болезнь Хантингтона
Галактоземия
Гемоглобин Е
Гемоглобин С
Гемохроматоз
Гликогенозы
Дальтонизм (часть вторая)
Дальтонизм (часть первая)
Дефицит 3 гидрокси-метил-глутарил-КоА лиазы
Дефицит 3-метилкротонил-коэнзим А карбоксилазы
Дефицит альфа 1 антитриптисина
Дефицит бета-кетотиолазы
Дефицит биотинидазы
Дефицит дигидропиримидин дегидрогеназы
Дефицит длинноцепочечной ацил-коэнзим А дегидрогеназы
Дефицит короткоцепочечной ацил-коэнзим А дегидрогеназы
Дефицит метилентетрагидрофолат редуктазы
Дефицит прекалликреин
Дефицит синтетазы голокарбоксилазы
Дефицит фактора ХI
Иминоглицинурия
Муковисцидоз
Мышечная дистрофия Дюшенна
Нейрофиброматоз
Органические ацидемии
Первичный системный дефицит карнитина
Перманентный неонатальный сахарный диабет
Перонеальная дистрофия Шарко-Мари-Тута (часть вторая)
Перонеальная дистрофия Шарко-Мари-Тута (часть первая)
Пропионовая ацидурия
Псевдополидистрофия Гурлера
Семейная вегетативная дисфункция
Семейная гиперхолестеринемия
Серповидно-клеточная анемия (часть вторая)
Серповидно-клеточная анемия (часть первая)
Синдром Ангельмана
Синдром Бартера
Синдром Блума
Синдром Дабина Джонсона
Синдром Дауна (часть вторая)
Синдром Дауна (часть первая)
Синдром Клайнфельтера-Рейфенштейна-Олбрайта
Синдром кошачьего крика
Синдром Криглера Найара
Синдром Леша-Наяна
Синдром Лойса-Дитца
Синдром Патау
Синдром Прадера-Вилли
Синдром Эдвардса
Тирозинемия
Тирозинемия І типа
Тирозинемия ІI типа
Тирозинемия ІIІ типа
Фенилкетонурия (ФКУ)
Фруктоземия
Х-сцепленный-ихтиоз
Целиакия (часть вторая)
Целиакия (часть первая)
Церебротендинальный ксантоматоз
Цистинурия
|